欧意交易所,欧意,欧意交易平台,欧意注册,欧意靠谱吗,欧意APP下载,欧易交易所官网,欧易下载,欧易下载链接,欧易apk下载,欧易网页版,欧易交易所,欧易下载,欧易官网,okx官网,欧易客户端下载外部挑战加剧,未来的投资框架应将中国医药行业置于全球视角之中,核心在于判断行业的比较优势是否 持续。中国医药行业参与全球竞争的优势主要在于:1)人口与内需优势。庞大的人口基数为中国医药行业带 来了广阔的内需市场。随着人们生活水平的提高、对健康的重视程度不断增加和老龄化的深入,国内医药市场 规模持续扩大。一方面为医药研发提供了充足的试验和数据支持,同时内需市场也为医药企业提供稳定的发展 基石,使其能够在国内需求不足的基础上,积累研发能力、生产技术和销售经验,并持续拓展海外市场,增强 在全球医药市场的影响力。2)制造与供应链优势。中国作为全球制造业大国之一,在医药制造领域拥有深厚 的产业基础和完善的供应链体系。从原材料供应到药品及设备的开发、生产等环节,都具备高效、稳定的特 点,既保证了国内的充足供应,还在国际市场上具有成本优势,能够为全球市场提供高性价比的医药终端产 品。3)创新能力快速提升。中国医药行业的创新能力近年来实现了质的飞跃。国内企业不断加大研发投入, 在多个领域取得了显著的创新成果,在国际上也具有一定的竞争力。在创新药研发和高端器械设备方面逐渐缩 小了与发达国家的差距,为参与全球竞争奠定了坚实的创新基础。
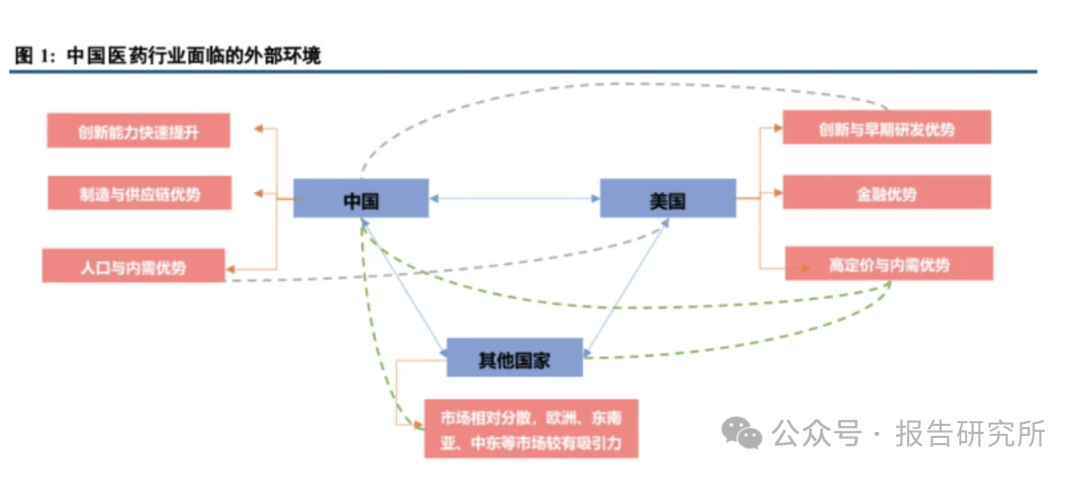
中国庞大的内需市场为医药企业发展的基石。各国的医药市场需求与人口结构关系密切,人口众多的国家 往往拥有较大的医药内需市场。从全球药品使用量来看(基于每日剂量,IQVIA 建模假设),2018-2023 年, 全球药品每日使用量从 2.96 万亿增加至 3.38 万亿,增加了 4140 亿个限定日剂量,预计到 2028 年将再增加 4000 亿个限定日剂量。分区域来看,预计未来五年中国、印度和亚太地区的销量增长最高,年复合增长率均 超过 3%,庞大的人口基数带来的医疗需求推动医药市场快速增长。同时,发达国家如美国、日本和欧洲各 国,尽管人口相对较少,卫生体系相对成熟,但人均医疗支出高、对创新药需求大,其医药市场较为发达。未 来,一方面中国庞大内需市场将作为为医药企业的基石和出海后盾,同时中国经济的发展和人均医疗支出水平 的提升将推动国内市场持续扩容。
中国医药行业具备显著的制造和供应链优势。根据工信部数据,我国规模以上医药工业企业超过 1 万家、 增加值占全部工业增加值比重约 4%,大宗原料药产量约占全球 40%,在研新药数量跃居全球第二位。根据 Cytiva 对于全球 22 个国家调查并发布的生物制药弹性指数,中国正迅速成为生物制药生产强国,供应链弹性 和生产敏捷性的得分高于全球平均水平;在全球生物制药供应链中,中国的原材料和加工材料占据主导地位。 根据 BCG的数据,2016 至 2020 年中国生物技术园区的数量增长了 50%,从大约 400 个增加到 600 个,总产 值增长超过 80%。
创新能力快速提升。中国医药行业的创新能力近年来实现了质的飞跃。国内企业不断加大研发投入,在多 个领域取得了显著的创新成果,在国际上也具有一定的竞争力。在创新药研发和高端器械设备方面逐渐缩小了 与发达国家的差距,为参与全球竞争奠定了坚实的创新基础。以 2025 年美国临床肿瘤学会(ASCO)年会为例, 今年口头汇报研究有 73 项为中国研究,各专场分布情况分别为:口头摘要专场为 32 项,摘要速递专场为 33 项,临床科学研讨会为 8 项。就摘要重磅程度而言,广受关注的 Late Breaking Abstract(LBA)中,中国研究 为 11 项,数量和占比相比往年都有明显提升。
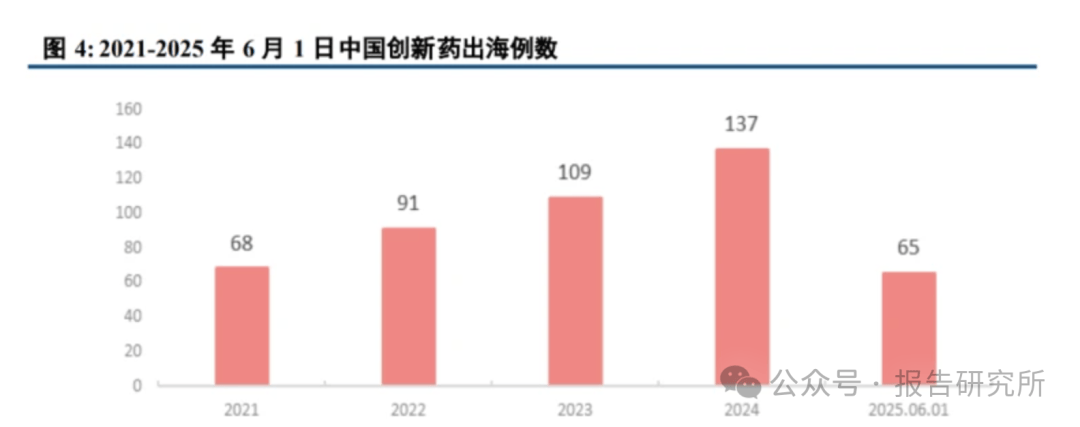
中国资产出海数量持续提升。根据 Insight 数据库,中国创新药资产国际化(转让方在国内,受让方在海外) 的数量从 2021 年的 68 例提升到 2024 年的 137 例,2025 年截止 6 月 1 日已经授权 65 例,根据现有趋势判断, 2025 年国际化授权数量有望超越 2024 年。我们认为,国际化授权数量的持续提升证明中国资产的逐步走强,未 来国际化数量有望实现进一步提升。
“自然指数”持续提升,中国科研力量持续进步。作为衡量科研力量的重要参考,“自然指数”是国际知 名的科研绩效评价工具,由 Springer Nature 集团于 2014 年推出,旨在通过追踪全球高质量自然科学期刊的论文 发表情况,评估国家、机构和学科领域的科研产出水平。根据统计数据,中国和美国的“自然指数”份额占比自 2020 年以来一直是第二和第一,但中国的份额呈现上涨趋势,美国呈现下降趋势。我们认为这一指数反映出中 国在基础科研上的持续高效进步,也证明中国在科技力量上的持续推进得到了验证,在此背景下,我们认为未 来中国创新力量将会持续迸发新的成果。
美国制药产业链依赖海外供应。根据 FDA 统计,2021 年 3 月,所有 FDA 注册的 FDF(finished dosage forms,可以认为是制剂)生产设施中有 52%在美国境外,73%的 FDA 注册 API 生产设施在美国境外。
美国仿制药产业链对海外依赖更高。从仿制药情况来看,在 FDA 注册的 ANDA 仿制药生产设施中,63% 位于美国境外,87%的 FDA 注册生产仿制药中使用的 API 的生产设施位于美国境外。
美国国内 120 种关键药品的分析:一半没有本土供应链。美国 HHS 对 120 种关键药物进行分析(其中 118 种来自 FDA 的 2020 年基本药物清单),结论是:1)50%的药物没有任何美国国内 API 生产设施;2)4% 的药物在美、欧、加没有任何 API 生产设施;3)8%的药物只能被外包到一个大洲进行生产;4)对于其中 50 种药物,其 70%的 API 设施位于亚洲。
美国在创新和早期研发方面积累较多、优势显著,使其在医药领域数据库的建立和维护上具有较强的影响 力。例如,美国主导的数据库包括 ClinicalTrials、PubChem、IQVIA 等,涵盖了临床试验注册、化学物质信 息、药物综合信息等多个方面,为美国的医药研发提供数据支持的同时,也对全球医药研究产生积极作用。目 前中国在药物研发与分子信息类数据库方面已有一定成果,预计后续会进一步加大在数据库建设方面的投入, 加强数据共享和利用,推动国内医药行业的发展,以更好地参与全球竞争。
医药行业关税具有三方面显著特征:1)关税政策具备明显的阈值特征,超过一定比例的关税可能导致贸 易量急剧下降甚至接近停滞,可能导致相应品类出现短缺风险。在阈值之上再提升关税比例带来的边际影响变 小。2)全球化产业链带来的复杂性:近年来全球化背景下产业链深度嵌合,使得关税的影响变得更加复杂。 医药行业作为全球化程度较高的领域,其前端研发、原材料采购、制剂生产制造以及产品销售等环节均跨越国 界。复杂的产业关联使得单一国家关税政策的调整的影响,需要在全球产业链国际分工中观察影响。3)医药 涉及人道主义,关税征收相对谨慎:医药行业因其涉及人类健康与生命安全,属于人道主义范畴,在关税征收 上通常相对谨慎。但医药行业仍面临一定的关税挑战,一些国家为了保护本国医药制造产业或提升供应链稳定 性,可能会实施特殊的关税政策或非关税壁垒。
全球化产业链带来的供应链复杂性:以大型跨国药企(MNC)主要生产基地为例,其生产基地广泛分布 于世界各地,如美国、欧洲、亚洲等主要地区。每个公司都在多个国家设有核心生产场地,例如辉瑞的生产场 地遍布美国、欧洲、亚太,多数 MNC 在中国同样有生产场地布局。生产场地的分布一方面反映了各地区的竞 争优势(制造成本、供应链配套),还涉及到不同地区在人口、市场需求方面的匹配。
医药行业关税的特征:征收相对谨慎,但仍有挑战。2025 年 4 月美国实施的“对等关税”政策中,医药 行业通过豁免清单实现了部分产品的关税豁免:1)化学制剂与生物制品大部分豁免:化药制剂、疫苗、抗体 等生物制品大部分均被纳入豁免清单,但含胰岛素、去甲麻黄碱及其盐、抗疟疾活性成分的未配定剂量药品, 以及相关已配定剂量药品仍被征税。2)原料药大部分豁免:大部分原料药被豁免,但布洛芬、去甲伪麻黄 碱、芬太尼前体(4-ANPP)及麦角新碱等特定原料药未被纳入豁免。3)医疗设备与耗材全面征税:医用耗 材、敷料、医疗设备及零部件、康复用品等未获豁免,需全额缴纳对等关税。特别是,注射器、针头、医用手 套、口罩等医用物品此前已经被加征了 301 关税,这些产品将会在原有关税基础上叠加适用对等关税。4)部 分药品生产原料受限:酒石酸、柠檬酸、甲硫氨酸等药物生产原材料未被豁免,但植物提取物(如芸香苷及其 衍生物)被列入豁免范围。 制药行业关税征收目前处于 232 调查过程中。美东时间 2025 年 4 月 1 日,美国商务部以确定进口药品和 药物成分及其衍生产品对国家安全的影响为由,根据《1962 年贸易扩展法》第 232 条发起调查。调查范围包 括仿制药和非仿制药成药、医疗对策,以及关键成分(如药物活性成分和关键起始物料及其衍生产品)。该调 查关注重点如下:1. 美国目前和预计对药品和药物成分的需求;2. 美国国内药品和药物成分生产能够满足国 内需求的程度;3. 外国供应链,特别是主要出口商在满足美国对药品和药物成分需求方面的作用;4. 美国集 中从少数供应商进口药物及药物成分的相关风险;5. 外国政府补贴和掠夺性贸易做法对美国制药业竞争力的 影响;6. 由于外国不公平贸易做法和国家支持的过度生产而人为压低药品和药品成分价格的经济影响;7. 外 国限制出口的可能性,包括外国将其对药品供应的控制武器化的能力;8. 提高国内生产药品和药品成分的能 力以减少对进口依赖的可行性;9. 现行贸易政策对国内生产药品和药品成分的影响,以及是否有必要采取额 外措施,包括关税或配额,以保护国家安全;10. 其他相关因素。
中国医药制造业进出口情况:制药产业链直接对美敞口有限。2024 年我国医药产品进出口贸易额 1993.76 亿美元,同比增长 2.13%,其中进口额 914.12 亿美元,同比下降 2%,出口额 1079.64 亿美元,同比增长 5.9%。从市场角度来看,2024 年我国对“一带一路”市场的医药出口额达 444.66 亿美元,同比增长 7.7%,对 欧盟市场的医药出口额超 200 亿美元。美国市场方面出口额为 190.47 亿美元,占中国医药出口比例为 17.6%。 对美国进口额为 150.57 亿美元,占中国医药进口比例为 16.5%。中国医药产业链直接对美敞口有限。
中美对于原产地认定均采取完全获得和实质性改变标准,预计后续各国对原产地的认定都会更加严格。中 美目前对于原产地认定整体规则框架基本相同,均基于完全获得和实质性改变两条,差异主要体现在各自的优 惠国贸易协定等内容。根据中华人民共和国国务院颁布的条例,目前中国对于进出口货物原产地的认定主要有 两条标准:1)“完全获得”:完全在一个国家(地区)获得的货物,以该国(地区)为原产地;2)“实质性改 变”:两个以上国家(地区)参与生产的货物,以最后完成实质性改变的国家(地区)为原产地。美国原产地规则 由美国国土安全部的美国海关和边境保护局 (CBP,Bureau of Customs and Border Protection) 管理。1) 完全获得:所有美国非优惠原产地规则计划都采用“完全获得”的标准,用于完全由特定国家/地区的种植、 产品或制造的商品。2)实质性改变:另一方面,所有美国非优惠原产地规则计划都对全部或部分由来自多个 国家/地区的材料组成的商品采用“实质性转换”标准。在大多数非优惠计划中,实质性转换标准是根据具体 情况适用的,并且它是基于名称/特性/使用方法的变化。包括税则归类变更(CTC)、区域价值成分 (RVC)、特定加工工艺标准。在关税壁垒提升的背景下,预计各国对于原产地的认定都会更加严格。

